En el 2018 por Resolución Ministerial de Salud Nº 623 se crea en el ámbito del Ministerio de Salud, dependiente de la Unidad de Coordinación General del mismo, la Comisión Nacional de Evaluación de Tecnologías Sanitarias (CONETEC). Las funciones inherentes a la Coordinación General de CONETEC se asignan al titular de la Unidad de Coordinación General del Ministerio de salud, y como Coordinador Operativo de la misma, al Secretario de Coberturas y Recursos de Salud. La Comisión estará integrada por un representante designado por el Ministerio de Salud, un representante designado por el Consejo Federal de Salud (Co.Fe.Sa.), un representante designado por la Superintendencia de Servicios de Salud y un representante de la Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (ANMAT). También se a invitar a formar parte de la Comisión Nacional de Evaluación de Tecnologías de Salud, con “carácter ad honorem”, a un representante por el Instituto Nacional de Servicios Sociales para Jubilados y Pensionados (INSSJP), un representante por las Obras Sociales Nacionales, un representante por las Obras Sociales Provinciales, un representante por las Entidades de Medicina Prepaga, un representante por las asociaciones de pacientes y un representante por la Defensoría del Pueblo de la Nación. http://servicios.infoleg.gob.ar/infolegInternet/anexos/305000-309999/308377/norma.htm
La CONETEC está integrada por representantes de los siguientes organismos e instituciones:
- Consejo Federal de Salud (COFESA),
- Superintendencia de Servicios de Salud (SSS),
- Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (ANMAT),
- Ministerio de Salud de la Nación, que ejerce además la Coordinación a través de la Subsecretaría de Medicamentos e Información Estratégica y de sus asesores,
- Instituto Nacional de Servicios Sociales para Jubilados y Pensionados (INSSJP),
- Obras Sociales Nacionales (OSN),
- Obras Sociales Provinciales (COSSPRA),
- Entidades de Medicina Prepaga (EMP9,
- Defensoría del Pueblo de la Nación,
- Asociaciones de Pacientes.
Estructura y flujo de trabajo de la CONETEC:

La participación de todos los integrantes en la CONETEC es con carácter “ad honorem” y adaptada a los diferentes espacios de interacción donde sus aportes sean requeridos.
La CONETEC no cuenta con un presupuesto propio asignado, depende del presupuesto del Ministerio de Salud de la Nación.
Para mayor información: https://www.argentina.gob.ar/sites/default/files/conetec_-_anexo_i._manual_operativo_2020.pdf
La CONETEC, cuenta con la asesoría técnica de instituciones académicas y científicas independientes con experiencia en la temática para integrar los Grupos de Trabajo:
- Universidad ISALUD (ISALUD)
- Instituto de Efectividad Clínica y Sanitaria (IECS)
- Red Argentina de Evaluación de Tecnologías Sanitarias (RedArETS)
- Centro Universitario de Farmacología de la Universidad Nacional de la Plata (CUFAR – UNLP)
- Instituto de Medicina para la Seguridad Social y Evaluación Tecnológica (IMSSET – UBA).
La CONETEC, es miembro de RedETSA, junto con otras organizaciones del país como son el CUFAR, el IECS, y la RedARETS.
El país cuenta con sus propias directrices o guías nacionales para la elaboración de los informes de ETS. Se pueden encontrar en: https://www.argentina.gob.ar/sites/default/files/4-manual-ets-conetec.pdf.
No cuentan con guías nacionales para la adaptación de informes de ETS de otros países y no realizan adaptaciones regularmente.
Aspectos operativos del proceso de ETS:
En primer lugar la recepción de las propuestas de tecnologías a ser evaluadas; anualmente la CONETEC mediante un mecanismo abierto y participativo recibe propuestas de TS a evaluar a través de un llamado público en la página web. En segundo caso, el listado de las TS es priorizado según la Herramienta de Priorización y al final del proceso se elabora un cronograma para los siguientes meses. El listado final de TS a evaluar es decidido por la Mesa de Priorización. Para comenzar el proceso de ETS de una TS, la CONETEC debe definir: el enfoque de la evaluación definiendo población, compradores y desenlaces; los actores de interés a ser convocados; los responsables de la elaboración y redacción del informe de ETS y el cronograma de trabajo.
Transparencia: Cuenta con declaración de conflicto de intereses. En el siguiente enlace se puede descargar el Acuerdo de reserva y uso confidencial de la información y el Formulario de declaración de conflictos de interés potencial: https://www.argentina.gob.ar/salud/conetec/funcionamiento
La CONETEC invita a pacientes, cuidadores y usuarios del sistema de salud a participar de la Mesa de Pacientes. Las convocatorias de la Mesa de Pacientes están destinadas a pacientes, cuidadores, familiares y usuarios del sistema de salud interesados en aportar su visión sobre la tecnología de salud (medicamento, instrumento, técnicas y procedimientos clínicos y quirúrgicos) o la condición de salud que la CONETEC esté evaluando. La información que aportarán está referida a puntos de vista, opiniones y expectativas sobre: la experiencia de vida con la condición de salud, el cuidado de una persona con esa condición de salud, la experiencia de recibir atención en el sistema de salud argentino, los beneficios suministrados por un tratamiento, la magnitud de los efectos no deseados y la comparación con otros tratamientos, la aceptabilidad y preferencias de los diferentes tratamientos y sus modos de administración. La CONETEC invita a participar a las personas por medio de un formulario para cada ETS que se está evaluando. Guía para la Mesa de pacientes: https://www.argentina.gob.ar/sites/default/files/5-guia-mesa-pacientes.pdf
Evaluaciones de efectividad, Respuestas rápidas de cobertura, Revisiones sistemáticas, Evaluaciones económicas.
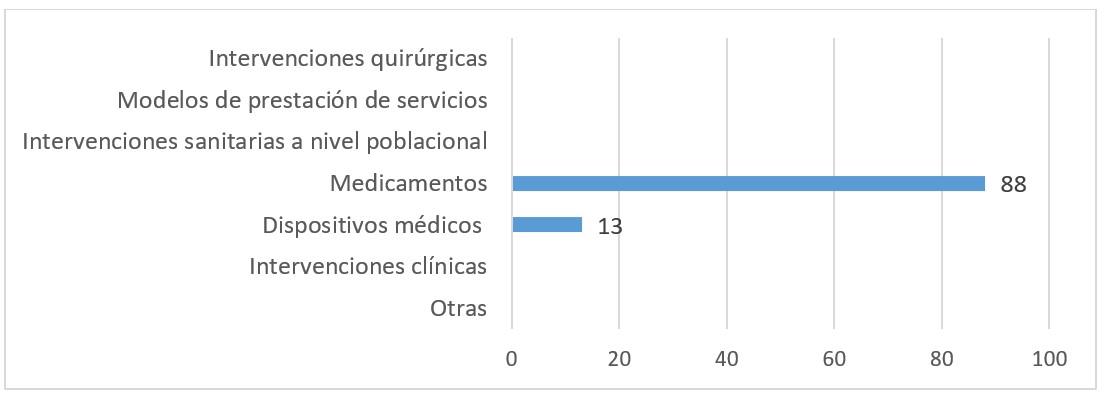
La CONETEC genera dos formatos de informes: Informes de Evaluaciones de Tecnologías Sanitarias (IETS) e Informes de Respuesta Rápida (IRR). Las ETS son evaluaciones integrales que incluyen consideraciones clínicas, económicas y de implementación, así como cuestiones éticas, legales y sociales. El Informe de ETS se llevará a cabo siguiendo la metodología establecida en el Documento técnico Nº4 (Manual metodológico para la escritura de reportes de evaluación de tecnologías sanitarias) según las siguientes fases: 1) Designación del Grupo de trabajo y enfoque; 2) Presentación inicial a
- Instituto de Efectividad Clínica y Sanitaria (IECS) Link a Brisa
- Red Argentina de Evaluación de Tecnologías Sanitarias (RedArETS) Link a Brisa
- Centro Universitario de Farmacología de la Universidad Nacional de la Plata (CUFAR – UNLP) Link a Brisa
- Instituto de Medicina para la Seguridad Social y Evaluación Tecnológica (IMSSET – UBA) Link a Brisa
- Universidad ISALUD (ISALUD) Link a Brisa
La norma (Resolución del Ministerio de Salud) establece que los resultados de la ETS deben ser tenidos en cuenta pero no son vinculantes en la toma de decisiones.
En primer lugar, para las tecnologías de salud que así lo requieran, la agencia reguladora del país (ANMAT) da aval e ingreso a las mismas para ser comercializadas en el país.
Los alcances de las coberturas en los diferentes subsistemas de salud coexistentes, las define cada subsector de financiamiento del país de acuerdo a definiciones propias (demanda, posibilidad de recupero de costos, protocolos propios de auditoría) no siempre basados en criterios taxativos de ETS.
El sistema de salud está en línea con la organización federal. Lo integran tres sectores: público, seguro social y privado. En cada provincia se administran con autonomía las funciones de rectoría, financiamiento y prestación de los servicios de salud. Su estructura se encuentra fragmentada y segmentada.
El sector público está conformado por los ministerios nacional y provinciales, y la red de hospitales y centros de salud públicos. Todos ellos prestan atención gratuita a quien lo demande, fundamentalmente a las personas en los quintiles de ingresos más bajos, sin seguridad social y sin capacidad de pago. Su financiamiento se acerca a 2,2% del producto interno bruto (PIB).
El sector del seguro social obligatorio está organizado en torno a las obras sociales, nacionales y provinciales. Las obras sociales nacionales son más de 200, e implican un gasto de 1,59% del PIB, y las 23 obras sociales provinciales cubren a los empleados públicos de su jurisdicción, abarcando 0,74% del PIB. El Instituto Nacional de Servicios Sociales para Jubilados y Pensionados cubre a las personas jubiladas del sistema nacional de previsión y a sus familias. Su cobertura ha alcanzado a 20% de la población, con un gasto que llega a 0,75% del PIB.
El sector privado está conformado por profesionales de la salud y establecimientos que atienden a demandantes individuales, además de los beneficiarios de las obras sociales y de los seguros privados.
Todas las obras sociales y el sector privado deben garantizar un conjunto de prestaciones de salud agrupadas en el Programa Médico Obligatorio (PMO).
El país cuenta con un Listado de Medicamentos Esenciales (LME) acorde a las recomendaciones de la OMS y actualizado, aunque no existe una exigencia legislativa para que los medicamentos seleccionados para la LME deban ser incluidos entre aquellos con cobertura garantizada en los conjuntos de prestaciones.
Existen en el país mecanismos de desinversión para las TS. Un ejemplo claro, dentro del subsistema de salud de las obras sociales, un evento de desinversión explícita fue implementada por el Instituto Nacional de Jubilados y Pensionados (PAMI) sacando de su cobertura los tratamientos combinados de glucosaminoglicanos / AINEs
En el país no existe una estrategia o plan Nacional de Uso Racional de Medicamentos y otras Tecnologías de Salud.
La prescripción por nombre genérico o Denominación Común Internacional (DCI) es obligatoria en el sector público del país y en la dispensa está permitida la sustitución por medicamentos multifuentes http://www.anmat.gov.ar/fna/25649.asp
El Servicio Nacional de Sanidad y Calidad Agroalimentaria (SENASA) creó en 2015 el Programa Nacional de Vigilancia de la Resistencia Antimicrobiana en animales destinados al consumo humano, con el objetivo de prevenir la generación y difusión de bacterias que resisten la acción de los antibióticos. La Estrategia Argentina para el Control de la Resistencia Antimicrobiana (aprobada a través de la Resolución Conjunta 834/2015 y 391/2015 del Ministerio de Salud y el ex Ministerio de Agricultura, Ganadería y Pesca https://www.argentina.gob.ar/normativa/nacional/resoluci%C3%B3n-834-2015-248651) y una Comisión Nacional integrada por los distintos organismos públicos con responsabilidad en la materia. Los ejes de trabajo para reducir el impacto de este fenómeno y limitar su propagación son: el fortalecimiento de la vigilancia clínica, microbiológica y farmacéutica, la regulación y fiscalización de la comercialización de antimicrobianos, la promoción del consumo racional y prudente, la detección precoz y el control de las infecciones en hospitales y en establecimientos agropecuarios, la promoción de la innovación en antimicrobianos. En el 2020 se creó además la Coordinación de Uso Apropiado de Antimicrobianos en el ámbito del Ministerio de Salud de la Nación con el fin de profundizar las acciones en favor de la lucha contra la RAM y en el uso adecuado de los antimicrobianos https://www.argentina.gob.ar/anmat/ram
Existen diferentes estructuras que desarrollan las guías a nivel nacional con estructuras funcionales propias e independientes. Por ejemplo, dentro del Ministerio de Salud hay varias áreas que elaboran guías (ej.: Enfermedades Crónicas, Calidad de Atención Médica) como así también otros organismos descentralizados (ej.: Superintendencia de Servicios de Salud), así como las actividades en sentido similar generadas por Sociedades Científicas independientes y también las GPC elaboradas por los ministerios de salud provinciales.
El país cuenta con una normativa nacional y guía para la elaboración y adaptación de GPC https://www.boletinoficial.gob.ar/detalleAviso/primera/218567/20191010?busqueda=1, pero no cuenta con una estrategia o política nacional para establecer mecanismos que faciliten la implementación de las GPC en los diferentes niveles. Tampoco se cuenta con un plan para actualizar las GPC que así lo requieran o evaluaciones de resultados de la implementación y utilización de las GPC. Las guías se elaboran informadas por la evidencia y desde el Ministerio de Salud nacional se enfoca en favorecer y fortalecer la metodología GRADE. Se han desarrollado varias guías utilizando esta metodología pero hace falta mayor institucionalización.
Si bien en la priorización para la elaboración de las GPC y en su propia elaboración, no se suele tener en cuenta los informes de ETS (no existe una concordancia en todos los casos), una vez que una TS es incorporada al PMO se pretende monitorear su indicación en las guías de práctica clínica y su correspondencia con las especificaciones de incorporación establecidas (edad de pacientes, estadio de patología, cumplimiento de criterios diagnósticos, tratamientos previos, etc.).
Enlaces para búsqueda de GPC del país:
https://www.argentina.gob.ar/salud/calidadatencionmedica/guiaspracticaclinica
https://bancos.salud.gob.ar/bancos/materiales-para-equipos-de-salud
El país cuenta con distintas formas de monitorear las Tecnologías de Salud: Sistemas de Farmacovigilancia, Sistemas de Tecnovigilancia, Servicios de auditoría, y además el subsector de la seguridad social nacional posee un sistema de tutelaje para el seguimiento de nuevas tecnologías.
El país cuenta con un proceso de priorización para definir los medicamentos y otras tecnologías sanitarias que serán evaluadas a nivel nacional. Este proceso tiene en cuenta las tecnologías sanitarias consideradas en las GPC. Para mayor información: https://www.argentina.gob.ar/sites/default/files/3-herramienta-priorizacion-conetec.pdf
La Agencia de Regulación del país es la Administración Nacional de Medicamentos, Alimentos y Tecnología Médica – ANMAT, cuyo papel en materia regulatoria es relevante. https://www.argentina.gob.ar/anmat
Acceso a las normativas vigentes que regulan la actividad de la ANMAT: http://www.anmat.gov.ar/webanmat/legislacion.asp
